Το μέλλον στην προγεννητική διάγνωση των γενετικών νόσων του εμβρύου: μη επεμβατική διάγνωση σε ελεύθερο DNA στο αίμα της εγκύου
H μη επεμβατική προγεννητική διάγνωση (MEΠΔ, NIPD: Non-Invasive Prenatal Diagnosis) στο αίμα της εγκύου είναι ένα από τα πλέον συναρπαστικά ερευνητικά πεδία της μοριακής ιατρικής την τελευταία δεκαετία. Η σημασία της ανάπτυξης και δυνατότητας εφαρμογής της στην κλινική πράξη είναι τεράστια, διότι δυνητικά θα είναι δυνατόν να προσφερθεί σε κάθε έγκυο χωρίς κανέναν κίνδυνο αποβολής.
Γράφουν οι
Βούλα Βελισσαρίου
Τμήμα Γενετικής και Μοριακής Βιολογίας MHTEΡΑ
Φίλιππος Πατσαλής
Ινστιτούτο Νευρολογίας και Γενετικής Κύπρου, Λευκωσία Κύπρος
Την τελευταία δεκαετία στο πεδίο της ΜΕΠΔ γενετικών νοσημάτων στο αίμα της εγκύου έχουν υπάρξει αλματώδεις εξελίξεις. Έχουν αναπτυχθεί διάφορες μεθοδολογικές προσεγγίσεις, οι οποίες αποδεικνύουν ότι η ΜΕΠΔ των χρωμοσωματικών ανωμαλιών του εμβρύου είναι εφικτή. Οι δύο πλέον υποσχόμενες μέθοδοι είναι η ΜΕΠΔ με την αλληλούχιση του DNA με αναλυτές επόμενης γενιάς και η ΜΕΠΔ με την ανοσοκατακρήμνιση μεθυλιωμένου DNA (MEDIP: Methylated DNA Immunoprecipitation) σε συνδυασμό με ποσοτική αλυσιδωτή αντίδραση της πολυμεράσης πραγματικού χρόνου (real time qPCR), ΜeDIP-real time PCR. Αμφότερες οι μέθοδοι έχουν επαληθευθεί με τυφλές μελέτες και έχουν >99% ακρίβεια. Η ΜΕΠΔ με τη δεύτερη μέθοδο, η οποία έχει αναπτυχθεί από ομάδα της Κύπρου σε συνεργασία με το τμήμα Γενετικής και Μοριακής Βιολογίας του ΜHTEΡΑ, βασίζεται στην ταυτοποίηση διαφορικά μεθυλιωμένων περιοχών στο DNA μεταξύ εμβρύου και εγκύου (DMRs: Differentially Methylated Regions), οι οποίες χρησιμοποιούνται για το διαχωρισμό των φυσιολογικών από τα παθολογικά έμβρυα. Έχουν ταυτοποιηθεί πάνω από 10.000 τέτοιες περιοχές για τα χρωμοσώματα 13, 18, 21, Χ και Υ με τη χρήση συστοιχιών ολιγονουκλεοτιδίων υψηλής διακριτικότητας (high resolution oligo-arrays), οι οποίες θα ήταν δυνατόν να χρησιμοποιηθούν για τη ΜΕΠΔ ανευπλοειδιών των χρωματοσωμάτων 13, 18, 21, Χ και Υ. Θα περιγραφεί εδώ η νέα μέθοδος, καθώς και τα πλεονεκτήματα και τα μειονεκτήματά της σε σχέση με τη ΜΕΠΔ με τη μέθοδο της αλληλλούχισης του DNA νέας γενιάς. Θεωρείται ότι αμφότερες οι μέθοδοι θα έχουν πολύ σύντομα εφαρμογή στην κλινική πράξη για τη διάγνωση των συχνότερων τρισωμιών του εμβρύου και στα επόμενα δέκα έτη για την προγεννητική διάγνωση όλων των συχνών, καθώς και σπανιότερων γενετικών νοσημάτων.
Ελεύθερο εμβρυϊκό DNA στο αίμα της εγκύου
Η ταυτοποίηση και απομόνωση του εμβρυϊκού DNA με μη επεμβατικές μεθόδους, το οποίο αναλύεται στη συνέχεια με μοριακές μεθόδους, είναι το κλειδί για την επιτυχή ΜΕΠΔ. Οι πρώτες ενδείξεις ότι θα ήταν δυνατή η ΜΕΠΔ στο αίμα της εγκύου υπήρξαν όταν το 1997 απομονώθηκαν εμβρυϊκά κύτταρα, καθώς και πολύ μικρή ποσότητα ελεύθερου εμβρυϊκού DNA (cffDNA) από το πλάσμα αίματος εγκύων. Αρχικά οι προσπάθειες ΜΕΠΔ για διάγνωση χρωμoσωματικών ανευπλοειδιών έγιναν με τη χρήση της τεχνικής φθορίζουσας υβριδοποίησης in situ (FISH) σε εμβρυϊκά κύτταρα που απομονώθηκαν από το αίμα της εγκύου. Όμως, ο εξαιρετικά μικρός αριθμός των εμβρυϊκών κυττάρων (1 στα 350.000 μητρικά κύτταρα), καθώς και η δυσκολία απομόνωσής τους, κατέστησαν την προσέγγιση αυτή αναποτελεσματική.
Αποτελεσματικότερη ήταν η χρήση του ελεύθερου εμβρυϊκού cffDNA στο αίμα της εγκύου για τη διάγνωση και μέτρηση DNA αλληλουχιών του εμβρύου, οι οποίες έχουν κληρονομηθεί αποκλειστικά από τον πατέρα και απουσιάζουν από το γονιδίωμα της εγκύου, όπως αυτές του χρωμοσώματος Υ στα άρρενα έμβρυα. Η προσέγγιση αυτή επέτρεψε την ανάπτυξη διαγνωστικών εξετάσεων για τον παράγοντα Rhesus του εμβρύου, καθώς και τη διάγνωση του φύλου του εμβρύου στην περίπτωση φυλοσύνδετου νοσήματος. Όμως, η ανάπτυξη ΜΕΠΔ για τις χρωμοσωματικές ανευπλοειδίες του εμβρύου, καθώς και για τα μονογονιδιακά νοσήματα, αποτελεί πολύ μεγαλύτερη πρόκληση, διότι το εμβρυϊκό DNA είναι μόλις το 3%-5% του συνολικού DNA στο πλάσμα του αίματος της εγκύου και είναι κατά 50% πανομοιότυπο με αυτό της μητέρας.
Η πρώτη διάγνωση χρωμoσωματικής ανευπλοειδίας εμβρύου σε DNA το οποίο απομονώθηκε από το πλάσμα αίματος εγκύου, αφορούσε στην τρισωμία 18. Επιτεύχθηκε το 2006 με τη χρήση μεθόδου που βασίζεται σε επιγενετικές τροποποιήσεις του DNA με τη μεθυλίωση, διαδικασία η οποία ως γνωστό καταστέλλει την έκφραση των γονιδίων. Ειδικότερα, βασίζεται στη χρήση διαφορικά μεθυλιωμένων περιοχών (DMRs) στο εμβρυϊκό και μητρικό DNA. Έκτοτε έχουν περιγραφεί αρκετές εναλλακτικές προσεγγίσεις που βασίζονται στη διαφορά στη μεθυλίωση των ίδιων περιοχών μεταξύ εμβρυϊκού και μητρικού DNA, με τεχνικούς όμως περιορισμούς, οι οποίοι δεν επέτρεψαν την ανάπτυξη μιας ακριβούς και αξιόπιστης μεθόδου. Προκειμένου να ξεπεραστούν οι παραπάνω τεχνικές δυσκολίες, η ομάδα μας ανέπτυξε μια νέα επιγενετική μέθοδο ΜΕΠΔ των χρωμoσωματικών ανωμαλιών του εμβρύου, την ανοσοκατακρήμνιση μεθυλιωμένου DNA (MEDIP: Methylated DNA Immunoprecipitation) σε συνδυασμό με ποσοτική αλυσιδωτή αντίδραση της πολυμεράσης πραγματικού χρόνου (real time qPCR), τη MeDIP- qPCR πραγματικού χρόνου, με τη χρήση ειδικά επιλεγμένων DMRs, η οποία έχει μεγάλη ευαισθησία και αξιοπιστία.
ΜΕΠΔ του συνδρόμου Down με τη μέθοδο MEDIP- qPCR πραγματικού χρόνου
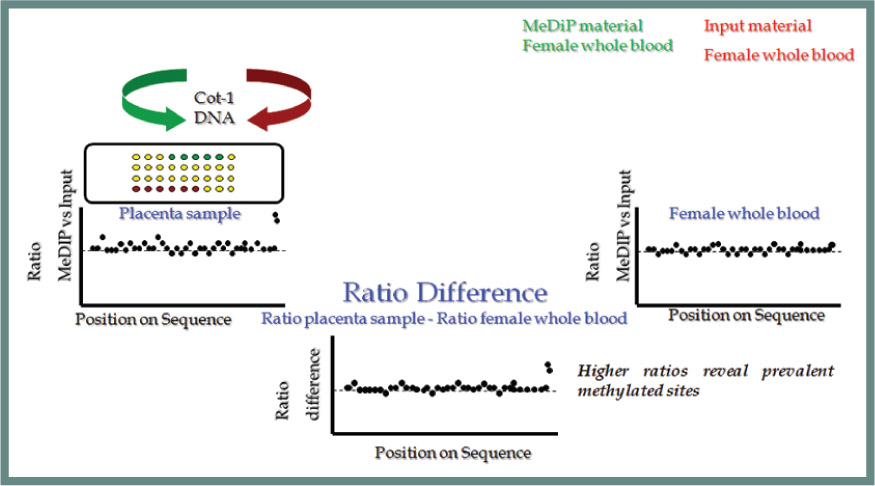
H ταυτοποίηση νέων DMRs στα χρωμοσώματα 13, 18, 21, Χ και Υ πραγματοποιήθηκε με τη χρήση της ανοσοκατακρήμνισης μεθυλιωμένου DNA και της υψηλής διακριτικότητας συστοιχιών ολιγονουκλεοτιδίων (ΜeDIP on a Chip)όπως φαίνεται στο σχήμα 1. Αρχικά πραγματοποιήθηκε ανοσοκατακρήμνιση DNA αίματος μη εγκύου γυναίκας και DNA πλακούντων πρώτου και δευτέρου τριμήνου σε δύο διαφορετικά πειράματα με τη χρήση ειδικού αντισώματος για τις περιοχές CpG του DNA, οι οποίες μεθυλιώνονται. Οι εμπλουτισμένες (ΜeDIP DNA, σχήμα 1) και οι μη εμπλουτισμένες (input DNA, σχήμα 1) σε μεθυλίωση περιοχές του DNA στα δείγματα αίματος και πλακούντων απομονώθηκαν και στη συνέχεια υβριδοποιήθηκαν σε ειδικό πλακίδιο με υψηλής διακριτικότητας συστοιχίες ολιγονουκλεοτιδίων (high resolution oligo-array, σχήμα 1). Το πλακίδιο-πλατφόρμα είναι ειδικά σχεδιασμένο με DNA αλληλουχίες των χρωμοσωμάτων 13, 18, 21, Χ και Υ. Η αναγνώριση των DMRs πραγματοποιήθηκε με τη χρήση του αλγορίθμου SW-ARRAY. Απομονώθηκαν συνολικά πάνω από 10.000 υποψήφια DMRs για τα χρωμοσώματα 13, 18, 21, Χ και Υ. Περίπου 2.000 βρίσκονται στο χρωμόσωμα 21. Από αυτά επελέγησαν 12 με βάση τα εξής κριτήρια: η επιλεγμένη περιοχή πρέπει να είναι υπερμεθυλιωμένη στον πλακούντα και υπομεθυλιωμένη στο αίμα της εγκύου, η κατάσταση μεθυλίωσης πρέπει να είναι ίδια στον πλακούντα πρώτου και τρίτου τριμήνου και, τέλος, τα επίπεδα μεθυλίωσης πρέπει να είναι πάνω από ένα κατώτατο όριο, το οποίο καθορίζεται από την ανάλυση με τις υψηλής διακριτικότητας συστοιχίες ολιγονουκλεοτιδίων.
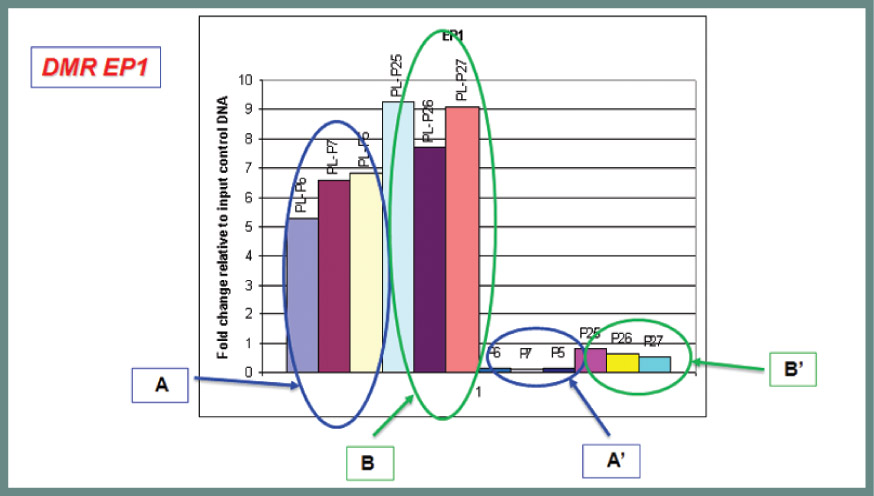
Προκειμένου να αποδειχθεί ότι τα παραπάνω επιλεγμένα DMRs είναι κατάλληλα για τη διάγνωση του συνδρόμου Down στο αίμα της εγκύου, εξετάστηκε μεγάλος αριθμός δειγμάτων. Στο σχήμα 2 φαίνεται η αυξημένη μεθυλίωση στον πλακούντα κυήσεων με σύνδρομο Down σε σχέση με εκείνη σε φυσιολογικές κυήσεις και αντίστοιχα η αυξημένη μεθυλίωση στο αίμα εγκύων με παθολογικές κυήσεις. Τα παραπάνω αποτελέσματα και η στατιστική ανάλυση των διαφορών επέτρεψαν την ανάπτυξη της νέας μεθόδου ΜΕΠΔ του συνδρόμου Down στο αίμα της εγκύου. Στο εξεταζόμενο δείγμα αίματος της εγκύου γίνεται αρχικά εμπλουτισμός των υπερμεθυλιωμένων περιοχών του εμβρυϊκού DNA με ανοσοκατακρήμνιση και στη συνέχεια για καθένα από τα παραπάνω επιλεγμένα DMRς γίνεται μέτρηση της μεθυλίωσης. Στη συνέχεια για κάθε DMR εξάγεται ένας λόγος σε σχέση με το μέσο όρο των μετρήσεων της μεθυλίωσης σε φυσιολογικά δείγματα (XEP – σχήμα 3). Mε τη χρήση του στατιστικού λογισμικού SPSS v16.0, σχεδιάστηκε η διαγνωστική εξίσωση: D = – 6.331 + 0.959 XEP4 + 1.188 XEP5 + 0.424 XEP6 + 0.621 XEP7 + 0.028XEP8 + 0.387 XEP10 – 0.683 XEP11 + 0.897 XEP12, όπου XEP είναι οι λόγοι για κάθε DMR. Όταν η τιμή D είναι >0, το δείγμα είναι παθολογικό, ενώ όταν είναι <0, είναι φυσιολογικό.
Εφαρμογή της ΜΕΠΔ για το σύνδρομο Down
Η νέα μέθοδος εφαρμόστηκε σε δείγματα περιφερικού αίματος εγκύων, οι οποίες προσήλθαν για λήψη χοριακών λαχνών μεταξύ της 11ης-13ης εβδομάδας της κύησης στο ΜΗΤΕΡΑ, λόγω αυξημένου κινδύνου κύησης με χρωματοσωματική ανωμαλία. Κατόπιν ενημέρωσης και ενυπόγραφης συγκατάθεσης της εγκύου, πραγματοποιήθηκε αιμοληψία πριν από τη λήψη των χοριακών λαχνών. Στη συνέχεια, αφού έγιναν γνωστά τα αποτελέσματα της επεμβατικής προγεννητικής διάγνωσης, η νέα μέθοδος εφαρμόστηκε σε 40 δείγματα συνολικά, εκ των οποίων 14 είχαν διαπιστωμένη τρισωμία 21, ενώ 26 ήταν φυσιολογικά. Η νέα μέθοδος διέγνωσε τόσο τα παθολογικά όσο και τα φυσιολογικά έμβρυα με 100% ευαισθησία και 100% ειδικότητα.
Η ΜΕΠΔ στην κλινική πράξη
Στην παρούσα φάση δύο μέθοδοι έχουν αναπτυχθεί και έχουν επαληθευτεί με 100% ακρίβεια. Η πρώτη βασίζεται στην αλληλούχιση του DNA με αναλυτές επόμενης γενιάς και η δεύτερη στην ανοσοκατακρήμνιση μεθυλιωμένου DNA (MEDIP) σε συνδυασμό με qPCR πραγματικού χρόνου. Αμφότερες οι μέθοδοι έχουν επαληθευθεί σε κλινικές μελέτες. Η μέθοδος ΜΕΠΔ με αλληλούχιση του DNA έχει επαληθευθεί σε δύο ανεξάρτητες κλινικές μελέτες. Στην πρώτη, σε 753 δείγματα με 100% ευαισθησία και 97,9% ειδικότητα. Στη δεύτερη, σε 1.696 δείγματα, με 98,6% ευαισθησία και 99,8% ειδικότητα. Η Cεπιγενετική μέθοδοςE με ανοσοκατακρήμνιση μεθυλιωμένου DNA (MEDIP) σε συνδυασμό με real time qPCR επαληθεύτηκε σε 175 δείγματα με 100% ευαισθησία και 99% ειδικότητα.
Συγκρίνοντας τις δύο μεθόδους παρατηρούνται τα εξής: Αμφότερες θεωρούνται ακριβείς με ευαισθησία και ειδικότητα άνω του 99%. Η μέθοδος ΜΕΠΔ με αλληλούχιση του DNA, εφόσον έχει επαληθευθεί σε μεγάλο αριθμό δειγμάτων, αναμένεται να εφαρμοστεί πρώτη στην κλινική πράξη. Για τη δική μας Cεπιγενετική μέθοδοE ΜΕΠΔ βασισμένη στη διαφορική μεθυλίωση, προκειμένου να αρχίσει η εφαρμογή της στην κλινική πράξη, σχεδιάζεται να προηγηθεί κλινική μελέτη με 1.000 δείγματα, η οποία υπολογίζεται να έχει ολοκληρωθεί εντός ενός έτους. Αμφότερες οι μέθοδοι είναι δυνατόν να εφαρμοστούν από τη 10η εβδομάδα της κύησης, με χρόνο απάντησης 15-21 ημέρες για τη ΜΕΠΔ με αλληλούχιση του DNA και 6-7 ημέρες για τη ΜΕΠΔ με μεθυλίωση. Όσον αφορά στην πολυπλοκότητα και στο κόστος, η ΜΕΠΔ με αλληλούχιση του DNA είναι σημαντικά πολυπλοκότερη και ακριβότερη (περίπου 1.900 ευρώ), καθώς απαιτεί ειδικό και πιο δαπανηρό εργαστηριακό εξοπλισμό, ενώ η ΜΕΠΔ με μεθυλίωση θα κοστίζει περίπου 400 ευρώ, είναι απλούστερη στην εφαρμογή της και ο απαιτούμενος εξοπλισμός αποτελεί μέρος του βασικού εξοπλισμού ενός εργαστηρίου μοριακής βιολογίας.
Η ΜΕΠΔ γενετικών νοσημάτων στο μέλλον
Από τη δεκαετία του 1970, η προγεννητική διάγνωση παρέχεται μέσω των επεμβατικών μεθόδων της λήψης χοριακών λαχνών (τροφοβλάστης), της αμνιοπαρακέντησης και της ομφαλοκέντησης με χρωματοσωματική ανάλυση και μεθόδους ανάλυσης του DNA. Η αλματώδης πρόοδος της τεχνολογίας και των μεθόδων, ειδικά την τελευταία δεκαετία, επέτρεψε τη θεαματική βελτίωση της διακριτικής ικανότητας της ανάλυσης του γονιδιώματος, με αποτέλεσμα την ταυτοποίηση βλαβών του DNA ακόμη και στο επίπεδο της μιας βάσης. Από τον καρυότυπο, ο οποίος ανιχνεύει τις συχνότερες χρωμοσωματικές ανωμαλίες και αναδιατάξεις, προχωρήσαμε στη διάγνωση συνδρόμων, τα οποία οφείλονται σε μικροελλείμματα και μικροδιπλασιασμούς με τη μέθοδο FISH, στη διάγνωση ακόμη περισσοτέρων αλλαγών στο DNA με κλινική σημασία με τη μέθοδο των συστοιχιών με CGH (array CGH) και, τέλος, στην αναγνώριση όλων των αλλαγών στο DNA ακόμη και στο επίπεδο της μιας βάσης με τους DNA αναλυτές επόμενης γενιάς.
Τα τελευταία 20 έτη, πολλές ερευνητικές ομάδες έχουν προσπαθήσει να μετατρέψουν την προγεννητική διάγνωση των γενετικών νοσημάτων σε μια διαδικασία ασφαλή για την έγκυο και το έμβρυο με την παροχή της ΜΕΠΔ. Σήμερα, το 2012, προβλέπεται ότι αρχίζει μια νέα εποχή. Με τη βοήθεια των μεθόδων ΜΕΠΔ, οι οποίες περιγράφηκαν, και τη συνεχή αναβάθμιση που θα ακολουθήσει, προβλέπεται ότι τα επόμενα 10 έτη με μια απλή αιμοληψία στην έγκυο θα είναι δυνατή η διάγνωση όλων των αλλαγών στο DNA, οι οποίες έχουν ως αποτέλεσμα την παθολογία του εμβρύου τόσο σε χρωμoσωματικό επίπεδο όσο και σε επίπεδο γονιδίων.
Eυχαριστίες
Επιθυμούμε να εκφράσουμε τις ευχαριστίες μας σε όλες τις εγκύους κυρίες, οι οποίες συναίνεσαν και κατέστη δυνατή η πραγματοποίηση των κατάλληλων δοκιμών, προκειμένου να αναπτυχθεί η νέα αυτή μέθοδος. Επίσης, ευχαριστίες σε όλους τους συνεργάτες μας, οι οποίοι συνετέλεσαν στην επιτυχία του εγχειρήματος. Τέλος, στις διοικήσεις του Ινστιτούτου Νευρολογίας και Γενετικής Κύπρου, καθώς και του ΜΗΤΕΡΑ, οι οποίες εμπιστεύθηκαν τις επιστημονικές μας ομάδες, παρέχοντας τη δυνατότητα να πραγματοποιηθούν οι κατάλληλες δοκιμές.
Σχήμα 2. Για το δείκτη DMR EP1, αριστερά φαίνεται η αυξημένη μεθυλίωση σε τρία διαφορετικά δείγματα πλακούντων κυήσεων με σύνδρομο Down (Β) σε σχέση με τρία δείγματα πλακούντων φυσιολογικών κυήσεων (Α). Δεξιά, για τον ίδιο δείκτη, φαίνεται η αυξημένη μεθυλίωση σε τρία διαφορετικά δείγματα αίματος εγκύων με έμβρυα με σύνδρομο Down (Β΄) σε σχέση με τρία δείγματα αιμάτων εγκύων με φυσιολογικά έμβρυα (Α΄).
Σχήμα 1. Ταυτοποίηση DMRs με τη χρήση της MeDIP και των υψηλής διακριτικότητας συστοιχιών ολιγονουκλεοτιδίων.
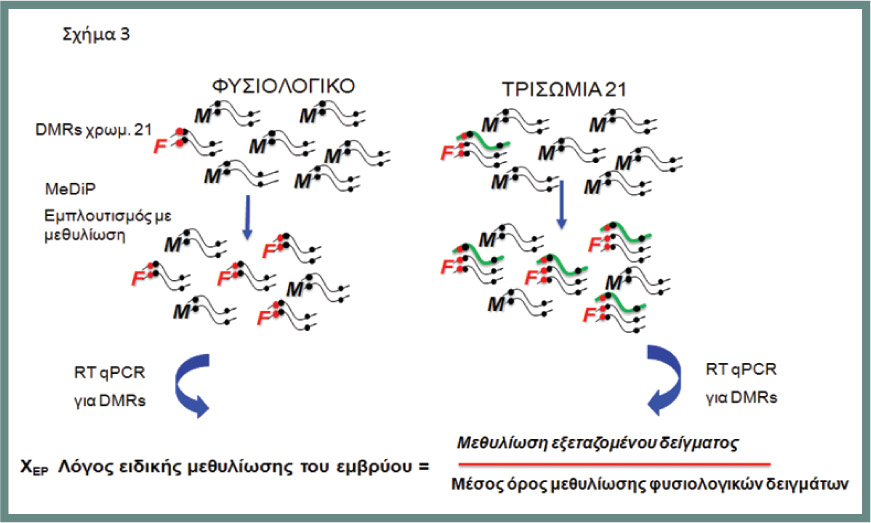
Σχήμα 3. Η μέθοδος ΜΕΠΔ με την ανοσοκατακρήμνιση μεθυλιωμένου DNA (MEDIP) σε συνδυασμό με real time PCR.
Δεκέμβριος 2012